L’incidence des infections, tout comme leur sévérité, est plus élevée chez les patients atteints de rhumatismes inflammatoires chroniques (RIC) qu’en population générale (1, 2). Plusieurs facteurs de risque infectieux ont été identifiés comme l’âge supérieur à 60 ans, un antécédent d’infection sévère, un échec à plusieurs traitements de fond, un traitement par corticoïde, un traitement ciblé, une maladie inflammatoire active (3). Les vaccins représentent un moyen de prévenir les infections et ont donc une place importante dans la prise en charge des patients atteints de RIC. Entre 2024 et 2025, des vaccins ont obtenu leur remboursement pour les patients atteints de RIC sous traitements immunosuppresseurs.
Vaccins recommandés dans les rhumatismes inflammatoires chroniques
En cas de RIC, les vaccins doivent être mis à jour selon le calendrier vaccinal et de préférence avant l’introduction d’un traitement immunosuppresseur (4).
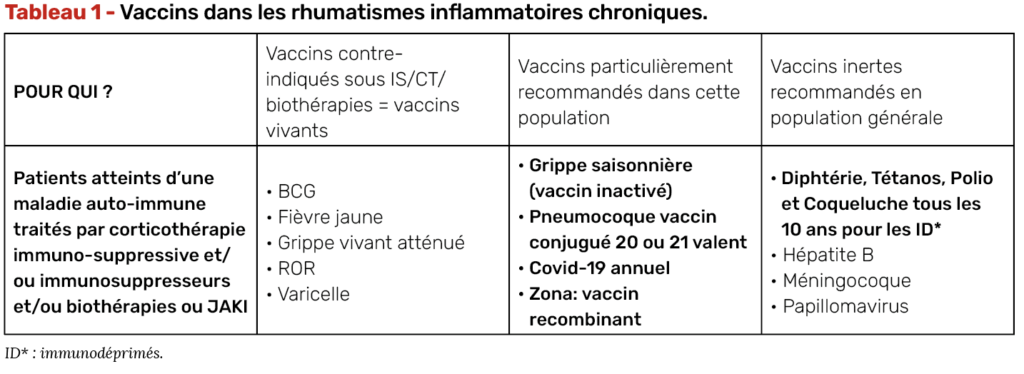
Chez les sujets immunodéprimés, en plus des vaccins habituels du calendrier vaccinal (sante.gouv.fr/prevention-en-sante/preserver-sa-sante/vaccination/calendrier-vaccinal), quatre vaccinations sont particulièrement recommandées (Tab. 1) :
• celles contre la grippe saisonnière et le Covid-19, tous les ans,
• celle contre le pneumocoque, dont le schéma vaccinal a été modifié en 2024 du fait des nouvelles recommandations du vaccin conjugué 20-valent VPC20 (Prevenar20®) ou VPC21 (Capvaxive®) chez l’adulte
• et celle contre le zona avec le vaccin recombinant Shingrix®.
La vaccination DTCaPolio
Chez l’adulte, les rappels DTPCaPolio sont recommandés aux âges fixes de 25, 45 et 65 ans, puis tous les 10 ans en utilisant un vaccin combiné tétanique, poliomyélitique et diphtérique (DTpolio). À l’âge de 25 ans, sera associée la valence coqueluche à dose réduite (DTCaPolio).
Chez les patients RIC
Pour les patients atteints de RIC, la vaccination DTP est recommandée plutôt tous les 10 ans que tous les 20 ans à partir de la date diagnostique du RIC.
La vaccination anti-pneumococcique
Depuis 2024 et la mise à disposition du vaccin conjugué pneumococcique 20-valent (VPC20), le schéma vaccinal comporte maintenant une seule dose du VPC20 (Prevnar20®) ou VPC21 (Capvaxive®) chez l’adulte.
Le schéma vaccinal avec le VPC20 ou VPC21 sera réalisé en fonction des situations suivantes :
• en cas de vaccination antérieure uniquement avec un vaccin pneumococcique polyosidique non conjugué 23-valent (VPP23), le VPC20 ou 21 peut être réalisé si la vaccination antérieure remonte à plus de 1 an ;
• si le patient a déjà reçu la séquence VPC13-VPP23 : une injection de VPC20 ou 21 en respectant un délai de 5 ans après la précédente injection.
Chez les patients RIC
Chez les patients atteints de RIC traités avec des médicaments ciblant l’immunité, la persistance de la protection vaccinale doit encore être évaluée pour pouvoir définir la meilleure stratégie de revaccination. En effet, si pour le sujet sain la vaccination par VPC20 ou 21 ne nécessite pas de rappel, pour les sujets atteints de RIC et traités avec des médicaments modulant l’immunité, la nécessité d’un rappel reste encore à préciser.
• Une étude observationnelle a montré que pour 302 patients atteints de RIC vaccinés avec le VPC7, le pourcentage des patients avec un titre des anticorps dirigés contre les sérotypes 6B et 23F était à 1,5 an en dessous du seuil de protection significativement diminué dans le groupe des PR recevant un traitement associant du méthotrexate (MTX) à un anti-TNF alors que les traitements n’avaient pas été modifiés pendant cette période de suivi (5).
• Dans l’étude VACIMRA, nous avons montré qu’il existe au cours de la première année une diminution progressive des titres des anticorps contre les 13 sérotypes du VPC13 (6).
Pour le VPC20 ou 21, nous n’avons pas encore les recommandations pour le rappel, mais il est probable que sur la base de ces études, un rappel sera à envisager chez les patients sous immunosuppresseurs.
Vaccinations contre la grippe et contre le pneumocoque
Les vaccinations contre la grippe saisonnière et contre le pneumocoque peuvent être réalisées le même jour en deux points d’injection différents. Ces deux vaccins sont aussi bien tolérés chez les patients atteints de rhumatismes inflammatoires que dans la population générale. Des interrogations concernant certains adjuvants contenus dans le vaccin de la grippe A ont été soulevées, mais les études réalisées lors de la pandémie de 2009 n’ont pas identifié plus d’effets secondaires ou d’exacerbations des rhumatismes inflammatoires ou de maladies auto-immunes (7).
La vaccination contre le zona
Le vaccin recombinant inerte contre le zona (VRZ ; Shingrix®) est administré en deux injections entre 1 et 6 mois d’intervalle. Le délai peut être raccourci à 1 mois par exemple si un traitement immunosuppresseur est envisagé. Le délai peut être allongé à 6 mois en cas de traitement déplétant les lymphocytes B (anti-CD20/rituximab) administré après la 1re dose.
Le VRZ a démontré sa capacité à prévenir un zona dans 97,2 % (IC 95 % : 93,7-99) avec une bonne tolérance (8). Cependant, des réactions au site d’injection sont plus fréquentes. Le vaccin recombinant adjuvé Shingrix® a obtenu une AMM le 23 mars 2018 pour la prévention du zona et des névralgies post-zostériennes chez les adultes de 50 ans et plus. Une extension d’indication a été octroyée en 2020, aux adultes de 18 ans ou plus, présentant un risque accru de zona.
Depuis 2024, ce vaccin est maintenant remboursé à 100 % en France pour les adultes âgés d’au moins 18 ans traités par immunosuppresseurs incluant les corticoïdes et en population générale, pour les sujets âgés de 65 ans et plus (recommandation HAS).
La vaccination anti-grippale
Le choix des souches virales contenues dans les vaccins est fait par l’Organisation mondiale de la santé (OMS) en fonction d’une veille sanitaire avec parfois des imprécisions dans l’identification de la souche qui sera à l’origine de l’épidémie (9). La vaccination anti-grippale est recommandée chez les patients atteints de RIC annuellement à partir du mois d’octobre. Des études ont révélé que la vaccination anti-grippale à haute dose a montré une protection supérieure au vaccin contre la grippe à dose standard contre les hospitalisations pour grippe ou pneumonie chez les adultes âgés de 65 ans (10). Ce vaccin antigrippal à haute dose pourrait être ainsi privilégié chez les patients immunodéprimés.
La vaccination anti-Covid19
Les premiers vaccins à avoir obtenu des autorisations en Europe sont le vaccin à ARN messager (ARNm) BNT162b ou Comirnaty® puis le vaccin mRNA 1273 ou Spikevax® (11, 12). Ces deux vaccins à ARNm sont réalisés avec deux doses administrées en intramusculaire à 1 mois d’intervalle. La vaccination est recommandée pour les patients atteints de RIC en raison du risque de développer une forme plus sévère, surtout en cas de traitements affectant l’immunité humorale ou cellulaire comme le MTX, le rituximab, l’abatacept et les corticoïdes prolongés. L’immunisation vaccinale combinée à l’immunisation naturelle post-infection Covid-19 a considérablement réduit les hospitalisations pour infection sévère à Covid-
19 au cours de la saison 2024-2025 alors que la couverture vaccinale contre le Covid-19 était tombée à 21 % chez les adultes de 65 ans et plus (www.santepubliquefrance.fr/maladies-et-traumatismes/maladies-et-infections-respiratoires/grippe/documents/bulletin-national/infections-respiratoires-aigues-grippe-bronchiolite-covid-19-.-bilan-de-la-saison-2024-2025).
La revaccination contre le Covid-19 est proposée au même moment que la vaccination anti-grippale dès le mois d’octobre. Ces vaccins saisonniers peuvent maintenant être réalisés par les pharmaciens et les infirmiers.
Un vaccin à ARNm contre la grippe et le Covid-19 vient d’obtenir son AMM de l’agence européenne du médicament. Ce vaccin, développé par Moderna (mCombriax®), permettrait de se protéger contre les deux virus avec une seule injection intra-musculaire (13).
La vaccination anti-virus respiratoire syncitial (VRS)
En France, 12 987 patients ont été hospitalisés entre 2012 et 2021 pour une infection secondaire au virus respiratoire syncitial (VRS), soit environ 4 000/an. Les patients étaient âgés en moyenne de 74 ans et 80 % avaient au moins une comorbidité, principalement des maladies respiratoires chroniques. Au total, 11 % ont été admis en réanimation et 7 % sont décédés. Enfin, 6,5 % des 12 033 patients vivants à la sortie du séjour initial ont été réadmis dans un service pour infection à VRS dans les 3 mois (14).
Il existe actuellement trois vaccins qui ont démontré leur efficacité dans la survenue d’une infection à VRS :
• deux protéiques, l’un avec adjuvant (Arexvy®)
• et l’autre sans (Abrysvo®),
• et un vaccin à ARNm (mResvia®) (15-17).
Les études observationnelles ont montré que la vaccination contre le VRS chez les sujets de plus de 60 ans réduisait de 75 à 80 % le risque d’une hospitalisation liée au VRS et contre les formes graves (18, 19).
Les indications vaccinales concer-nent actuellement les sujets de 75 ans et plus et ceux de 65 à 75 ans avec une comorbidité, sans qu’aucun vaccin ne soit aujourd’hui remboursé dans ces indications. Pour les patients immuno-déprimés, les recommandations sont encore attendues.
La vaccination contre le papillomavirus humain (HPV)
En France, le papillomavirus humain (HPV) est responsable chaque année de 6 400 cancers, principalement du col de l’utérus avec 2 900 cas (20). La vaccination contre HPV a démontré son efficacité sur la prévention de survenue de cancers du col utérin.
• À partir des registres suédois, l’incidence des cancers du col invasifs a été calculée dans l’ensemble de la population des jeunes filles/femmes de 10 à 30 ans, entre les femmes vaccinées et non vaccinées. Sur une population de plus de 1,6 million d’individus, il existe une réduction significative du risque de cancer du col invasif estimée à 88 % lorsque la vaccination est réalisée avant 17 ans et de 53 % si elle est réalisée entre 17 et 30 ans (21).
• Ces résultats ont été confirmés en 2025 dans une méta-analyse de la Cochrane qui montre que la vaccination contre HPV, surtout lorsqu’elle est administrée avant 16 ans, réduit fortement l’incidence des lésions cervicales de haut grade et du cancer du col de l’utérus, sans augmentation démontrée des effets indésirables graves (22).
• Dans la polyarthrite rhumatoïde (PR), le risque de cancer du col de l’utérus est deux fois plus élevé qu’en population générale et pourrait être favorisé par l’immunosuppression induite par les traitements (23, 24).
En pratique
La vaccination contre HPV comporte trois doses à réaliser entre 11 et 19 ans avec un rattrapage possible jusqu’à 26 ans pour les filles comme pour les garçons. La vaccination est possible jusqu’à 45 ans après une évaluation individuelle. Elle est recommandée même après une infection HPV, car elle limite les infections futures en particulier contre les souches associées au risque de cancer du col.
Pour les patients qui ont reçu une greffe de cellules souches hématopoïétiques (CSH), la série vaccinale doit être réadministrée jusqu’à l’âge de 45 ans si la greffe de CSH a eu lieu après l’administration du vaccin contre le HPV.
Fenêtre d’opportunité vaccinale et traitements immunosuppresseurs
Avant initiation d’un traitement immunosuppresseur
Est-il envisageable de réaliser les vaccins avant l’initiation du traitement immunosuppresseur chez des patients avec une PR active sans grever le contrôle du RIC ?
L’essai VACIMRA
L’essai VACIMRA a permis de répondre à cette question dans la PR (6). Dans cette étude ouverte et randomisée, 276 adultes atteints de PR active (DAS28 > 3,2), n’ayant jamais reçu de MTX, de léflunomide, d’autres traitements ciblés modificateurs de la maladie (tDMARDs), ni de vaccination anti-pneumococcique préalable, ont été inclus. Les participants ont été répartis aléatoirement en deux groupes :
• le premier recevait le MTX immédiatement en même temps que le vaccin VPC13 (groupe “immédiat”),
• tandis que le second commençait le MTX 1 mois après la vaccination (groupe “différé”).
Les résultats ont montré un taux significativement plus élevé de réponse immunitaire dans le groupe différé après 1 mois et une activité fonctionnelle des anticorps qui demeurait plus élevée dans le groupe différé pour la majorité des sérotypes après 1 an de suivi. Fait important, aucune différence significative n’a été observée entre les groupes concernant les scores d’activité de la maladie ou les schémas thérapeutiques.
Ces résultats soutiennent l’intérêt de différer de 1 mois l’instauration du MTX, quelle que soit l’activité du RIC, pour réaliser les vaccinations afin d’optimiser la réponse immunitaire, et sans compromettre le contrôle de la maladie sur 1 an de suivi. Toutefois si l’activité du RIC le nécessite, le traitement immunosuppresseur peut être initié sans délai.
Cas des vaccins vivants
Pour les vaccins vivants, de manière générale, il est conseillé de mettre à jour les vaccinations par vaccins vivants atténués avant le début de tout traitement immunosuppresseur (4). Les vaccins concernés sont le BCG, le ROR, ceux dirigés contre la fièvre jaune, la varicelle, la poliomyélite par voie buccale, la dengue, le chikungunya. La vaccination par un vaccin vivant doit toujours être précédée d’une évaluation de la balance bénéfices (protection vaccinale)/risques (infection vaccinale ou risques liés à une possible réactivation de la maladie en cas d’arrêt des traitements). Les vaccins vivants sont contre-indiqués chez les femmes enceintes.
Après initiation d’un traitement immunosuppresseur
Stratégie d’arrêt des traitements pour les vaccins saisonniers
Les vaccins contre la grippe et le Covid-19 étant répétés tous les ans, les patients atteints de RIC seront vaccinés alors qu’ils seront sous traitements immunosuppresseurs qui peuvent affecter la réponse vaccinale.
Les études
Les essais cliniques disponibles se sont intéressés aux réponses vaccinales induites après la suspension temporaire du MTX, avant et/ou après l’immunisation. Dans l’ensemble, les essais contrôlés randomisés ont démontré qu’une interruption transitoire du MTX pendant 1 à 2 semaines après la vaccination anti-grippale et après la vaccination contre le SARS-CoV-2 améliorait la réponse en anticorps chez les patients atteints de PR (25-27). Les adaptations thérapeutiques testées n’ont pas compromis le contrôle de la maladie. Toutefois, deux études ont rapporté une augmentation du nombre de poussées de PR dans le groupe ayant interrompu le traitement pendant 2 semaines après la vaccination anti-grippale, ainsi qu’après la seconde dose de vaccin contre le Covid-19.
Les recommandations
La proposition d’arrêter les traitements de fond pour réaliser les vaccins inactivés n’est pas consensuelle, car les recommandations Eular proposent de poursuivre les traitements (4), alors que les recommandations de l’ACR proposent, pour réaliser un vaccin contre le Covid-19 et la grippe, un arrêt temporaire du traitement pour le MTX et les JAKi (7 jours après le vaccin), et l’abatacept (7 jours avant et 7 jours après) (28).
En pratique
En pratique, on peut envisager, chez un patient en rémission de son RIC, un arrêt temporaire du traitement de fond pendant 1 à 2 semaines après la vaccination anti-grippale et anti-Covid-19 pour améliorer la réponse aux vaccins. Cela ne doit cependant pas représenter un frein à la réalisation de ces vaccins chez des patients que nous avons déjà du mal à vacciner. En effet, les vaccins inertes peuvent être administrés même sous traitement de fond. Ainsi, les professionnels de santé non spécialisés en rhumatologie (par exemple, les pédiatres, généralistes et les internistes) sont encouragés à administrer le vaccin contre la grippe, le Covid-19, même s’ils ne savent pas s’il faut suspendre le MTX, puis à consulter le rhumatologue du patient plutôt que de manquer une occasion de vaccination. En revanche, il existe un consensus pour le rituximab qui réduit considérablement la réponse anticorps des vaccins. Pour cette raison, il est recommandé de réaliser les vaccins au moins 4 mois après la dernière perfusion de rituximab. L’idéal serait de placer les vaccins 2 à 4 semaines avant la perfusion de rituximab, si l’activité de la maladie le permet.
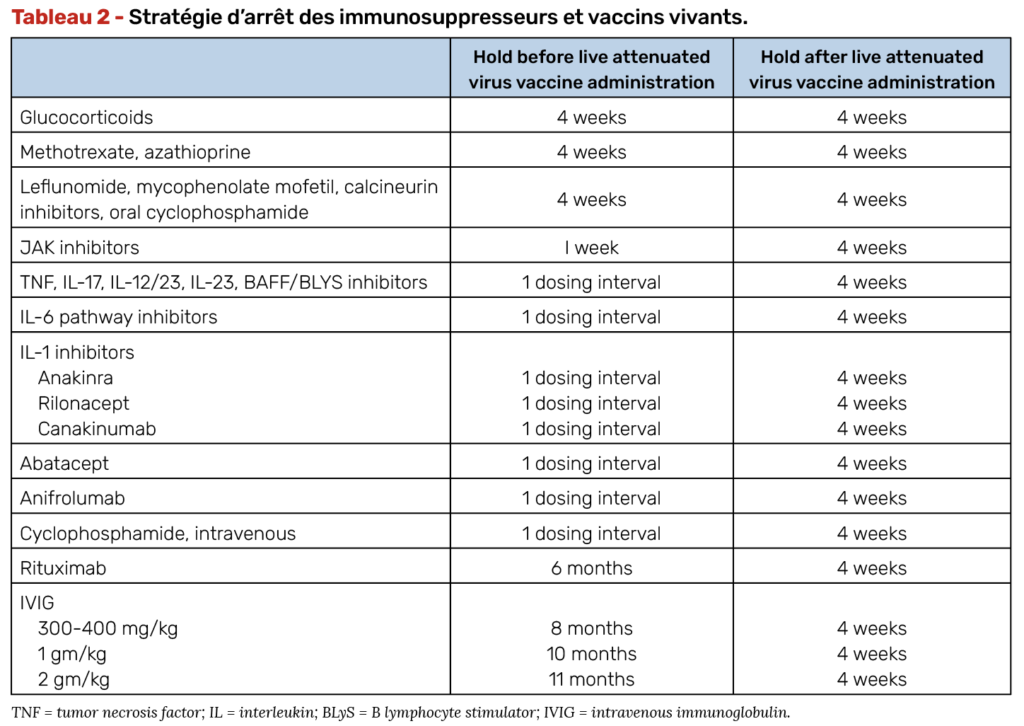
Stratégie d’arrêt des traitements pour les vaccins vivants
Des études ont montré une tolérance correcte des vaccins vivants contre la varicelle/zona ou anti-amarile, sous traitements de fond classiques et/ou biologiques (29, 30). Cependant, en raison des limites de ces études observationnelles ou rétrospectives, les vaccins vivants restent contre-indiqués en cas de traitements de fond classiques et biologiques par le Haut Conseil de santé publique (HCSP) et les recommandations Eular et ACR. En effet, un arrêt de ces traitements est nécessaire avant l’administration d’un vaccin vivant. Le HCSP proposait un arrêt des immunosuppresseurs 3 mois avant la réalisation d’un vaccin vivant et une reprise du traitement immunosuppresseur 1 mois après. Ce délai de 4 mois empêche de réaliser la majorité des vaccins vivants sans exposer le patient à une poussée de sa maladie inflammatoire.
Les recommandations américaines
Les recommandations américaines (ACR) de 2022 proposent des délais d’arrêt plus courts.
• Pour le MTX et le léflunomide, un arrêt de 1 mois avant la réalisation d’un vaccin vivant est proposé (31).
• Pour les traitements ciblés hors rituximab et JAKi, un arrêt correspondant à l’intervalle de temps entre deux administrations du biomédicament est recommandé avant d’administrer un vaccin vivant.
• Un délai de 6 mois entre la dernière perfusion de rituximab et la réalisation d’un vaccin vivant est proposé et 1 semaine pour les JAKi. Les traitements seront repris 1 mois après la réalisation d’un vaccin vivant.
• Pour les corticoïdes : jusqu’à la dose de 10 mg/j de prednisone depuis moins de 15 jours, un vaccin vivant atténué peut être administré sans restriction. Pour des assauts cortisoniques et pour des posologies de prednisone dépassant 10 mg/j > 15 j, les vaccins vivants contre la fièvre jaune, la varicelle et le ROR peuvent être envisagés 1 mois après l’arrêt des corticoïdes.
• Un traitement par hydrocortisone, une corticothérapie locale (intra-articulaire notamment) ou inhalée ne sont pas des contre-
indications à la vaccination par vaccins vivants.
Ces recommandations plus récentes permettent d’envisager plus facilement la réalisation d’un vaccin vivant.
Les recommandations européennes
Les recommandations européennes (Eular) actualisées sur la vaccination chez les patients atteints de maladies inflammatoires à médiation immune reprennent l’ensemble des principes généraux et des recommandations sur la vaccination des patients atteints de maladies inflammatoires chroniques. Elles sont en cours d’actualisation et seront présentées lors du congrès Eular 2026 à Londres.
L’auteur déclare avoir des liens d’intérêt avec Abbvie, Biogen, BMS, Boehringer Ingelheim, Celltrion, Lilly, Mylan/Viatris, Pfizer, Sanofi.
Bibliographie
1. Furer V, Rondaan C, Heijstek M et al. Incidence and prevalence of vaccine preventable infections in adult patients with autoimmune inflammatory rheumatic diseases (AIIRD): a systemic literature review informing the 2019 update of the EULAR recommendations for vaccination in adult patients with AIIRD. RMD Open 2019 ; 5 : e001041.
2. Doran MF, Crowson CS, Pond GR et al. Frequency of infection in patients with rheumatoid arthritis compared with controls: a population-based study. Arthritis Rheum 2002 ; 46 : 2287‑93.
3. Strangfeld A, Eveslage M, Schneider M et al. Treatment benefit or survival of the fittest: what drives the time-dependent decrease in serious infection rates under TNF inhibition and what does this imply for the individual patient? Ann Rheum Dis 2011 ; 70 : 1914‑20.
4. Furer V, Rondaan C, Heijstek MW et al. 2019 update of EULAR recommendations for vaccination in adult patients with autoimmune inflammatory rheumatic diseases. Ann Rheum Dis 2020 ; 79 : 39‑52.
5. Crnkic Kapetanovic M, Saxne T, Truedsson L, Geborek P. Persistence of antibody response 1.5 years after vaccination using 7-valent pneumococcal conjugate vaccine in patients with arthritis treated with different antirheumatic drugs. Arthritis Res Ther 2013 ; 15 : R1.
6. Morel J, Dernis E, Roux C et al. Effect of a 1-month methotrexate delay on pneumococcal vaccine immunogenicity and disease control in patients with early rheumatoid arthritis (VACIMRA): an open-label randomised trial. Lancet Rheumatol 2025 ; 7 : e675‑86.
7. Elkayam O, Amir S, Mendelson E et al. Efficacy and safety of vaccination against pandemic 2009 influenza A (H1N1) virus among patients with rheumatic diseases. Arthritis Care Res 2011 ; 63 : 1062‑7.
8. Lal H, Cunningham AL, Godeaux O et al. Efficacy of an adjuvanted herpes zoster subunit vaccine in older adults. N Engl J Med 2015 ; 372 : 2087‑96.
9. Ntshoe GM, McAnerney JM, Tempia S et al. Influenza epidemiology and vaccine effectiveness among patients with influenza-like illness, viral watch sentinel sites, South Africa, 2005-2009. PLoS One 2014 ; 9 : e94681.
10. Johansen ND, Modin D, Pardo-Seco J et al. Effectiveness of high-dose influenza vaccine against hospitalisations in older adults (FLUNITY-HD): an individual-level pooled analysis. Lancet 2025 ; 406 : 2425‑34.
11. Baden LR, El Sahly HM, Essink B et al. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine. N Engl J Med 2021 ; 384 : 403‑16.
12. Polack FP, Thomas SJ, Kitchin N et al. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine. N Engl J Med 2020 ; 383 : 2603‑15.
13. Rudman Spergel AK, Wu I, Deng W et al. Immunogenicity and safety of influenza and COVID-19 multicomponentvaccine in adults ≥50 years. A randomized clinical trial. JAMA 2025 ; 333 : 1977-87.
14. Loubet P, Fernandes J, de Pouvourville G et al. Respiratory syncytial virus-related hospital stays in adults in France from 2012 to 2021: A national hospital database study. J Clin Virol 2024 ; 171 : 105635.
15 Walsh EE, Pérez Marc G, Zareba AM et al. Efficacy and safety of a bivalent RSV prefusion F vaccine in older adults. N Engl J Med 2023 ; 388 : 1465‑77.
16. Papi A, Ison MG, Langley JM et al. Respiratory syncytial virus prefusion F protein vaccine in older adults. N Engl J Med 2023 ; 388 : 595‑608.
17. Wilson E, Goswami J, Baqui AH et al. Efficacy and safety of an mRNA-based RSV PreF vaccine in older adults. N Engl J Med 2023 ; 389 : 2233‑44.
18. Payne AB, Watts JA, Mitchell PK et al. Respiratory syncytial virus (RSV) vaccine effectiveness against RSV-associated hospitalisations and emergency department encounters among adults aged 60 years and older in the USA, October, 2023, to March, 2024: a test-negative design analysis. Lancet 2024 ; 404 : 1547‑59.
19. Bajema KL, Yan L, Li Y et al. Respiratory syncytial virus vaccine effectiveness among US veterans, September, 2023 to March, 2024: a target trial emulation study. Lancet Infect Dis 2025 ; 25 : 625‑33.
20. Shield KD, Marant Micallef C, de Martel C et al. New cancer cases in France in 2015 attributable to infectious agents: a systematic review and meta-analysis. Eur J Epidemiol 2018 ; 33 : 263‑74.
21. Lei J, Ploner A, Elfström KM et al. HPV vaccination and the risk of invasive cervical cancer. N Engl J Med 2020 ; 383 : 1340‑8.
22. Henschke N, Bergman H, Buckley BS et al. Effects of human papillomavirus (HPV) vaccination programmes on community rates of HPV-related disease and harms from vaccination. Cochrane Database Syst Rev 2025 ; 11 : CD015363.
23. Foster E, Malloy MJ, Jokubaitis VG et al. Increased risk of cervical dysplasia in females with autoimmune conditions-Results from an Australia database linkage study. PLoS One 2020 ; 15 : e0234813.
24. Wadström H, Frisell T, Sparén P, Askling J. Do RA or TNF inhibitors increase the risk of cervical neoplasia or of recurrence of previous neoplasia? A nationwide study from Sweden. Ann Rheum Dis 2016 ; 75 : 1272‑8.
25. Park JK, Lee MA, Lee EY et al. Effect of methotrexate discontinuation on efficacy of seasonal influenza vaccination in patients with rheumatoid arthritis: a randomised clinical trial. Ann Rheum Dis 2017 ; 76 : 1559‑65.
26. Abhishek A, Peckham N, Pade C et al. Effect of a 2-week interruption in methotrexate treatment on COVID-19 vaccine response in people with immune-mediated inflammatory diseases (VROOM study): a randomised, open label, superiority trial. Lancet Rheum 2024 ; 6 : e92‑104.
27. Skaria TG, Sreeprakash A, Umesh R et al. Withholding methotrexate after vaccination with ChAdOx1 nCov19 in patients with rheumatoid or psoriatic arthritis in India (MIVAC I and II): results of two, parallel, assessor-masked, randomised controlled trials. Lancet Rheum 2022 ; 4 : e755‑64.
28. Curtis JR, Johnson SR, Anthony DD et al. American College of Rheumatology Guidance for COVID-19 vaccination in patients with rheumatic and musculoskeletal diseases: Version 3. Arthritis Rheumatol 2021 ; 73 : e60‑75.
29. Tricco AC, Zarin W, Cardoso R et al. Efficacy, effectiveness, and safety of herpes zoster vaccines in adults aged 50 and older: systematic review and network meta-analysis. BMJ 2018 ; k4029.
30. Oliveira ACV, Mota LMH, Santos-Neto LL et al. Seroconversion in patients with rheumatic diseases treated with immunomodulators or immunosuppressants, who were inadvertently revaccinated against yellow fever. Arthritis Rheumatol 2015 ; 67 : 582‑3.
31. Bass AR, Chakravarty E, Akl EA et al. 2022 American College of Rheumatology Guideline for vaccinations in patients with rheumatic and musculoskeletal diseases. Arthritis Care Res 2023 ; 75 : 449‑64.



