Les rhumatismes inflammatoires chroniques (RIC) – polyarthrite rhumatoïde (PR), spondyloarthrites (SpA), rhumatisme psoriasique (RPso) – sont associés à une morbi-mortalité accrue. Si le risque cardiovasculaire a longtemps occupé le devant de la scène, le risque oncologique constitue aujourd’hui un enjeu majeur, à la fois médical, médico-légal et psychologique. L’arrivée des biothérapies puis des traitements synthétiques ciblés a profondément transformé le pronostic fonctionnel et structural des RIC. Cependant, la modulation immunitaire prolongée qu’ils induisent soulève des interrogations quant à une possible altération de l’immunosurveillance tumorale.
La Société française de rhumatologie (SFR) a récemment publié des recommandations spécifiques sur l’évaluation et la gestion du risque de cancer avant l’initiation d’un traitement ciblé chez les patients atteints de RIC (1). Ces recommandations visent avant tout à aider le rhumatologue dans sa pratique quotidienne, en apportant un cadre clair d’évaluation du risque oncologique, sans complexifier inutilement la prise en charge ni retarder l’instauration d’un traitement efficace. Cet article propose une traduction pratique de ces recommandations pour le rhumatologue.
Risque de cancer lié aux RIC : facteurs liés à la maladie
Polyarthrite rhumatoïde
Épidémiologie et risques
La PR est associée à un excès de risque global de cancer estimé entre 15 et 25 % par rapport à la population générale selon les grandes cohortes et méta-analyses internationales (2). Ce surrisque n’est toutefois ni uniforme ni homogène selon les localisations tumorales.
• Il concerne principalement les lymphomes, en particulier les lymphomes B diffus à grandes cellules, dont le risque est multiplié par deux à trois selon les études.
• Les cancers pulmonaires présentent également un excès de risque significatif, souvent compris entre 30 et 50 %, en partie lié au tabagisme, mais aussi à l’inflammation chronique systémique et aux atteintes pulmonaires associées à la PR telles que la pneumo-
pathie interstitielle ou les anomalies bronchiques.
• Les cancers cutanés, notamment les cancers cutanés non mélanocytaires, ainsi que les cancers vésicaux, sont également plus fréquents.
À l’inverse, certaines localisations comme le cancer du sein ou de l’endomètre semblent moins représentées, possiblement en lien avec des facteurs hormonaux ou des mécanismes d’immunosurveillance particuliers.
Mécanismes physiopathologiques
L’élément central à retenir est que l’activité inflammatoire chronique apparaît comme le principal déterminant du risque oncologique dans la PR, davantage que l’exposition médicamenteuse elle-même. Plusieurs travaux ont démontré une relation étroite entre activité élevée et prolongée de la maladie et survenue de lymphomes. Les patients présentant une PR sévère, érosive et insuffisamment contrôlée sont ceux qui présentent le risque le plus élevé. À l’inverse, certaines données suggèrent une diminution de l’incidence des lymphomes à l’ère des biothérapies, parallèlement à une meilleure maîtrise de l’inflammation. Sur le plan physiopathologique, l’inflammation persistante favorise une stimulation antigénique chronique, une prolifération lymphocytaire prolongée, une production soutenue de cytokines proinflammatoires comme le TNF ou l’IL-6 et une instabilité génomique susceptible de favoriser la transformation maligne.
Ainsi, l’inflammation prolongée constitue un terrain propice à la lymphomagenèse indépendamment des traitements. En pratique, cela signifie qu’un contrôle insuffisant de la PR expose probablement davantage au risque de lymphome qu’un traitement ciblé efficace permettant de réduire l’activité inflammatoire.
Spondyloarthrites et rhumatisme psoriasique
Épidémiologie et risques
Dans les SpA et le RPso, le risque de cancer apparaît globalement comparable à celui de la population générale dans la majorité des grandes cohortes européennes et nord-américaines (3). Il n’existe pas d’augmentation marquée du risque de cancers solides majeurs tels que les cancers du sein, du côlon ou de la prostate. Néanmoins, certaines nuances doivent être apportées. Des signaux ont été rapportés concernant certaines hémopathies malignes, notamment les lymphomes et le myélome multiple, avec un excès de risque modéré et moins marqué que dans la PR. Cette augmentation pourrait être liée à l’inflammation chronique systémique ou à des formes plus sévères et prolongées de la maladie, même si les données restent hétérogènes selon les populations étudiées. Certaines cohortes asiatiques ont décrit des risques plus élevés, mais la transposition de ces résultats aux populations européennes doit être prudente en raison de différences génétiques et environnementales.
Dans le rhumatisme psoriasique
Dans le RPso, le signal le plus constant concerne les cancers cutanés non mélanocytaires (4). Ce surrisque semble largement lié au psoriasis cutané lui-même, à l’exposition cumulative aux ultraviolets et aux traitements antérieurs tels que la photothérapie, plutôt qu’au rhumatisme en tant que tel. Le risque de mélanome reste débattu et semble au maximum modérément augmenté.
En l’état actuel des connaissances, il n’y a pas d’indication à un dépistage oncologique extensif systématique chez les patients atteints de SpA ou de RPso en dehors des recommandations nationales habituelles. Une vigilance ciblée, en particulier dermatologique chez les patients avec atteinte cutanée importante ou antécédents d’exposition aux UV, apparaît suffisante.
Le rôle central des facteurs de risque classiques
Le risque oncologique des patients atteints de RIC ne peut être interprété uniquement à la lumière de la maladie ou des traitements prescrits. Il est également influencé par des facteurs de risque “classiques”, souvent plus fréquents dans cette population, tels que le tabagisme, l’âge, l’obésité ou certaines expositions environnementales. L’évaluation du risque de cancer doit donc s’inscrire dans une approche globale intégrant les caractéristiques démographiques, les habitudes de vie et les comorbidités du patient.
• Le tabagisme occupe une place centrale, en particulier dans la PR. Il est associé à un risque accru de cancers pulmonaires et vésicaux, mais également à une moindre réponse aux traitements, favorisant indirectement le maintien d’une inflammation chronique susceptible de contribuer à la lymphomagenèse.
• L’âge avancé constitue un autre déterminant majeur, lié à l’accumulation de mutations somatiques et à la diminution de l’immunosurveillance tumorale.
• L’obésité et le syndrome métabolique participent également à un état inflammatoire chronique de bas grade pouvant favoriser la carcinogenèse, tandis que certaines expositions environnementales, notamment aux ultraviolets ou à des toxiques inhalés, peuvent contribuer au risque tumoral dans des contextes particuliers.
• Enfin, les comorbidités cardiovasculaires et métaboliques, fréquentes dans les RIC, participent à un terrain global de vulnérabilité.
Ainsi, les facteurs de risque classiques doivent être systématiquement recherchés et intégrés à l’évaluation du risque oncologique, car ils peuvent modifier l’équilibre bénéfice/risque des traitements ciblés et orienter la stratégie thérapeutique, notamment chez les patients âgés, fumeurs ou présentant de multiples comorbidités.
Traitements des RIC et risque de cancer : synthèse pratique
Les recommandations SFR ne se limitent pas à une analyse descriptive du risque oncologique des différentes classes thérapeutiques. Elles proposent également une hiérarchisation des choix thérapeutiques chez les patients présentant un risque oncologique identifié.
Traitements de fond conventionnels synthétiques
Les traitements de fond conventionnels synthétiques (csDMARDs) conservent un profil oncologique globalement rassurant.
• Le méthotrexate n’est pas associé à une augmentation significative du risque global de cancer lorsqu’on ajuste sur l’activité de la maladie (5, 6). Les signaux observés pour les cancers cutanés non mélanocytaires et pour la persistance d’infection à HPV justifient une surveillance adaptée, mais ne remettent pas en cause son utilisation en pratique courante.
• Le léflunomide et la sulfasalazine ne sont pas associés à un signal oncologique robuste et reproductible à ce jour. Leur utilisation ne nécessite pas de précaution spécifique au-delà du respect des recommandations générales de dépistage.
Biothérapies
Les anti-TNF
Les anti-TNF constituent la classe pour laquelle le recul est le plus important. Les données issues des registres nationaux et internationaux n’ont pas montré d’augmentation du risque global de cancer (7-9). Un surrisque modéré de cancers cutanés non mélanocytaires et de lésions cervicales de haut grade est en revanche bien documenté, ce qui justifie une surveillance dermatologique et gynécologique adaptée.
Les inhibiteurs de l’IL-6
Les inhibiteurs du récepteur de l’IL-6 présentent un profil de sécurité oncologique rassurant, sans signal clair d’augmentation du risque tumoral dans les grandes cohortes (2). Ils constituent donc une option acceptable chez les patients présentant un risque oncologique accru.
Les autres biothérapies anti-cytokines
Les autres biothérapies anti-cytokines plus récemment introduites, notamment les inhibiteurs de l’IL-17 et de l’IL-23, disposent encore d’un recul plus limité, mais les données disponibles issues des essais cliniques, de leurs extensions et des registres de pharmacovigilance n’ont pas mis en évidence d’augmentation significative du risque de cancer, que ce soit pour les tumeurs solides ou les hémopathies malignes. L’incidence observée est généralement comparable à celle attendue dans les populations de référence. Toutefois, le recul reste inférieur à celui des anti-TNF et une surveillance à long terme demeure nécessaire, en particulier chez les patients présentant d’autres facteurs de risque oncologique.
Le rituximab
Le rituximab est fréquemment utilisé chez des patients présentant un antécédent oncologique ou un risque élevé. Les signaux rapportés dans certaines bases médico-
administratives semblent largement expliqués par un biais d’indication. En pratique, il est souvent considéré comme une option prudente chez les patients à haut risque, en particulier en cas d’antécédent d’hémopathie.
L’abatacept
L’abatacept est associé à un signal modéré, mais reproductible, d’augmentation du risque tumoral dans certaines études observationnelles, principalement porté par les cancers cutanés. Ce signal, bien que modeste en valeur absolue, conduit la SFR à recommander la prudence chez les patients présentant un antécédent de cancer ou un risque élevé de récidive.
Inhibiteurs de JAK
Les inhibiteurs de JAK constituent la seule classe pour laquelle un signal de surrisque de cancer a été mis en évidence dans un essai randomisé dédié (10). Ce signal concernait principalement des patients âgés, fumeurs ou porteurs de facteurs de risque cardiovasculaire, avec un excès observé notamment pour les cancers pulmonaires.
Sur cette base, chez les patients ayant un antécédent personnel de cancer ou une prédisposition génétique significative, les inhibiteurs de JAK (et l’abatacept) ne doivent être envisagés qu’en l’absence d’alternative thérapeutique adaptée et après discussion collégiale.
La recommandation 8 élargit cette prudence à certaines situations à haut risque, notamment chez les patients âgés de 65 ans ou plus et chez les fumeurs actifs ou anciens fumeurs, même en l’absence d’antécédent oncologique formel.
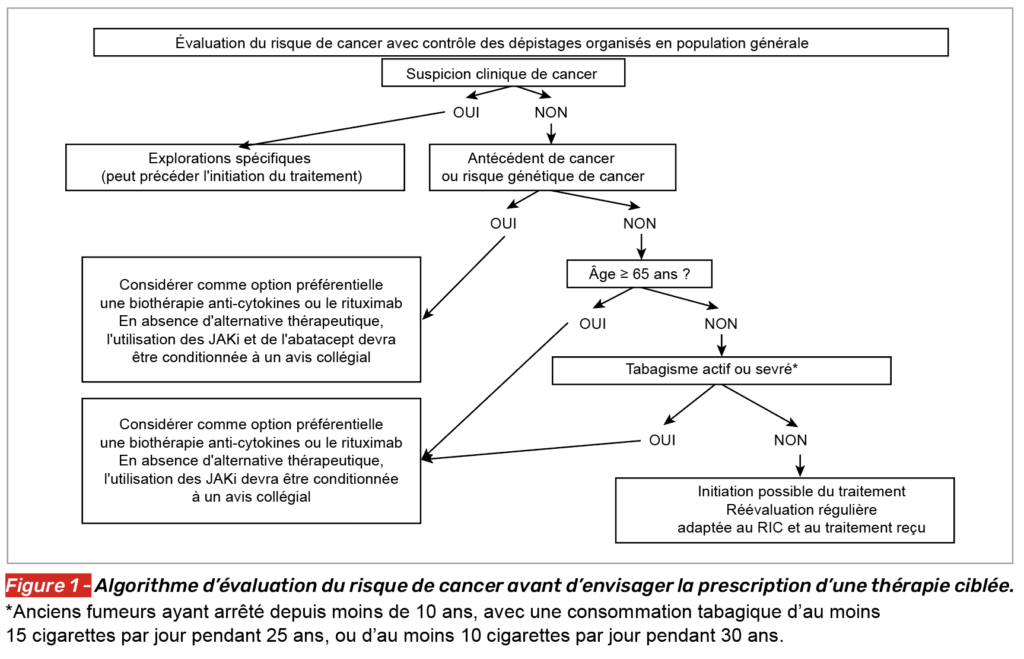
Intégration pratique de l’algorithme décisionnel (Fig. 1)
L’algorithme proposé par la SFR permet d’opérationnaliser ces recommandations en consultation (1). La première étape consiste à vérifier l’absence de suspicion clinique de cancer et à s’assurer que les programmes de dépistage organisés sont à jour.
• En cas de suspicion, des explorations spécifiques doivent précéder toute initiation de traitement ciblé.
• En l’absence de suspicion, l’évaluation repose sur trois axes :
1/ existence d’un antécédent personnel de cancer ou d’un risque génétique significatif ;
2/ âge ≥ 65 ans ;
3/ statut tabagique (actif ou ancien fumeur).
• En présence d’un antécédent de cancer ou d’un risque génétique élevé, les thérapies anti-cytokines (anti-TNF, anti-IL-6) ou le rituximab doivent être privilégiées. L’utilisation d’un inhibiteur de JAK ou de l’abatacept ne doit être envisagée qu’en l’absence d’alternative adaptée et après décision collégiale.
• Chez les patients sans antécédent oncologique, mais âgés de 65 ans ou plus, ou fumeurs actifs/anciens fumeurs, la prudence reste de mise. Les anti-cytokines ou le rituximab sont à considérer en première intention. L’utilisation des inhibiteurs de JAK doit être conditionnée à une analyse individualisée du rapport bénéfice/risque.
• En l’absence de facteur de risque identifié, l’initiation d’un traitement ciblé peut être envisagée selon les recommandations habituelles, avec une réévaluation régulière adaptée à la maladie et au traitement reçu.
Apports pratiques des recommandations SFR
Contrôle de l’activité de la maladie et sevrage tabagique
Les recommandations de la SFR soulignent que la prévention du risque de cancer chez les patients atteints de RIC ne repose pas uniquement sur les stratégies de dépistage. Elle implique également le contrôle optimal de l’activité de la maladie et la réduction des facteurs de risque modifiables, en particulier le tabagisme.
Le contrôle de l’inflammation
Le contrôle de l’inflammation constitue un objectif majeur, notamment dans la PR. Plusieurs études ont montré une association étroite entre activité inflammatoire persistante et risque accru de lymphome, en particulier pour les lymphomes B diffus à grandes cellules. L’inflammation chronique favorise en effet une stimulation antigénique prolongée, une prolifération lymphocytaire soutenue et une production persistante de cytokines pro-inflammatoires susceptibles de contribuer à la carcinogenèse.
Dans ce contexte, une stratégie thérapeutique visant la rémission ou une faible activité de la maladie pourrait indirectement contribuer à réduire le risque de certaines hémopathies malignes. Cette approche s’inscrit dans la stratégie treat-to-target, qui constitue aujourd’hui la base de la prise en charge des RIC.
Le tabagisme
Le tabagisme représente par ailleurs l’un des facteurs de risque modifiables les plus importants chez les patients atteints de RIC. Il est fortement associé à plusieurs localisations tumorales, notamment les cancers pulmonaires et vésicaux, et contribue également à la survenue et à la sévérité de la PR. Le tabac est également associé à une moindre réponse aux traitements de fond, en particulier aux biothérapies anti-TNF, favorisant indirectement le maintien d’une activité inflammatoire élevée.
Dans cette perspective, l’encouragement au sevrage tabagique doit être systématique au cours du suivi rhumatologique. L’orientation vers des programmes de sevrage, l’utilisation de substituts nicotiniques ou le recours à des traitements médicamenteux peuvent être proposés selon les situations.
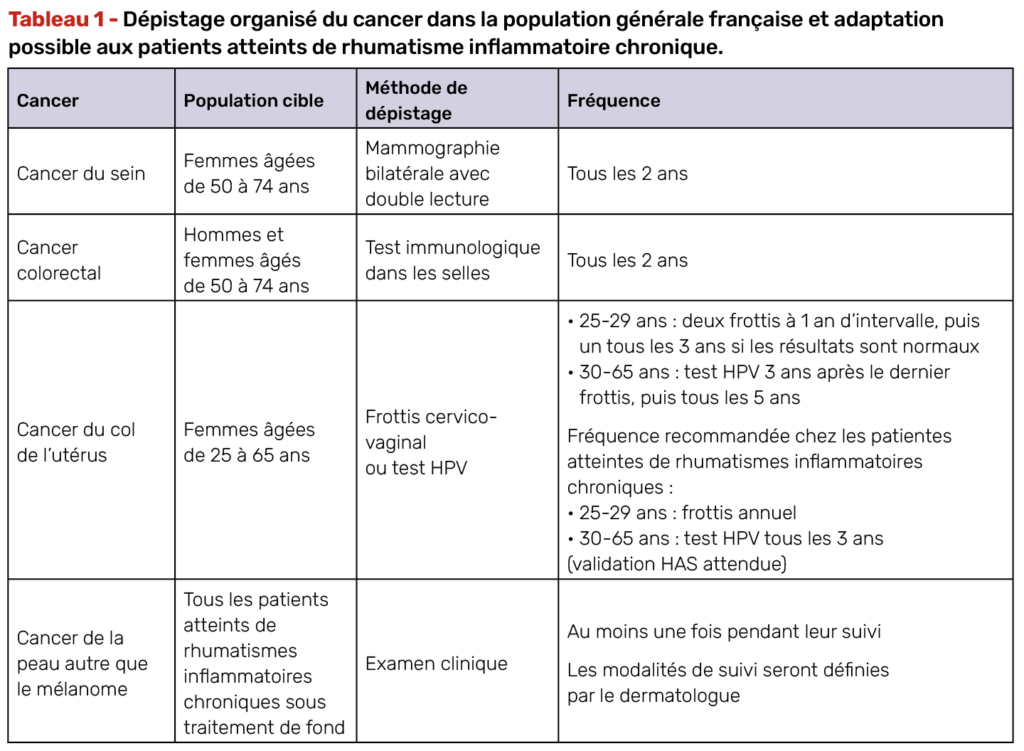
Dépistage des cancers (Tab. 1)
Les recommandations récentes de la SFR ne préconisent pas un sur-dépistage généralisé, mais insistent sur l’application rigoureuse et systématique des programmes nationaux de dépistage, avec des adaptations ciblées chez les patients sous traitements de fond conventionnels et ciblés (1). L’objectif est double : ne pas médicaliser excessivement ces patients, tout en évitant les oublis fréquents liés à la complexité de leur prise en charge.
Pour le cancer du sein
Pour le cancer du sein, le dépistage doit suivre les recommandations nationales en vigueur, avec mammographie tous les 2 ans entre 50 et 74 ans. Il n’existe pas de données justifiant un raccourcissement systématique des intervalles chez les patientes atteintes de RIC. L’enjeu pratique est surtout de vérifier que le dépistage est effectivement réalisé, car les patients suivis pour maladie chronique peuvent parfois négliger ces examens.
Pour le cancer colorectal
Le dépistage du cancer colorectal doit également être appliqué selon les modalités habituelles, avec test immunologique fécal tous les 2 ans à partir de 50 ans, ou coloscopie selon les recommandations en cas de facteur de risque spécifique. Là encore, les RIC ne justifient pas de stratégie différente en dehors des situations individuelles particulières.
Pour le cancer du col de l’utérus
Le cancer du col de l’utérus constitue un point plus spécifique. Chez les femmes atteintes de RIC recevant un traitement immunomodulateur prolongé, le risque de persistance d’infection à HPV et de progression vers des lésions intra-épithéliales de haut grade est augmenté. Les recommandations SFR suggèrent donc une surveillance plus rapprochée que dans la population générale. En pratique, cela peut se traduire par un intervalle raccourci (par exemple tous les 3 ans après 30 ans sous HPV test) et une vigilance accrue chez les patientes exposées de longue date aux immunosuppresseurs. Chez les femmes jeunes ayant initié un traitement immunomodulateur précocement, la discussion d’un dépistage anticipé peut se poser au cas par cas.
Pour les cancers cutanés
Le risque cutané fait également l’objet d’une attention particulière. Les cancers cutanés non mélanocytaires sont les plus fréquemment observés sous immunomodulation, en particulier chez les patients âgés ou exposés aux UV. Les recommandations préconisent au minimum une consultation dermatologique au cours du suivi, afin d’évaluer le risque individuel (phototype, antécédents, exposition solaire, traitements reçus) et de définir la fréquence ultérieure des contrôles. Cette approche individualisée est préférable à un dépistage systématique annuel pour tous. L’éducation à l’autosurveillance cutanée reste un élément clé.
Pour le cancer pulmonaire
Enfin, le dépistage du cancer pulmonaire ne fait pas encore l’objet d’une recommandation nationale généralisée, mais la vigilance doit être accrue chez les patients fumeurs ou anciens fumeurs atteints de PR, compte tenu du cumul de facteurs de risque (tabac, inflammation chronique, atteinte pulmonaire interstitielle). La participation aux programmes de dépistage lorsqu’ils sont proposés doit être encouragée.
L’ensemble de ces mesures rappelle que le rôle du rhumatologue ne consiste pas à se substituer au médecin traitant, mais à s’assurer que ces dispositifs sont bien activés et intégrés dans la stratégie globale de soins.
Vaccination HPV
La vaccination contre le HPV représente un levier préventif majeur dans cette population.
• Chez les patients de moins de 26 ans, le statut vaccinal doit être systématiquement vérifié. En cas de schéma incomplet ou absent, une vaccination de rattrapage doit être proposée, idéalement avant l’instauration d’un traitement immunomodulateur afin d’optimiser la réponse immunitaire.
• Chez les patients déjà sous traitement, la vaccination reste possible et recommandée, même si la réponse immunogène peut être légèrement diminuée. La balance bénéfice/risque demeure largement favorable.
Cette démarche s’inscrit dans une stratégie plus globale de prévention des cancers liés au HPV, incluant le col de l’utérus, mais également certaines localisations anogénitales et ORL.
Conclusion et perspectives
Le risque de cancer chez les patients atteints de RIC est multifactoriel et ne peut être attribué uniquement aux traitements ciblés. Il résulte d’une interaction complexe entre inflammation chronique, facteurs de risque individuels et immunomodulation thérapeutique. Les recommandations récentes de la SFR offrent un cadre pragmatique permettant d’évaluer ce risque, d’organiser le dépistage et d’adapter les choix thérapeutiques sans retarder l’instauration d’un traitement efficace.
En pratique
Pour le rhumatologue, l’enjeu est d’intégrer systématiquement cette évaluation dans la consultation, en tenant compte de l’âge, du tabagisme, des antécédents oncologiques et du contrôle de la maladie (Encadré 1). Une approche structurée permet de sécuriser la prescription des traitements ciblés tout en maintenant un contrôle optimal de l’inflammation.

Perspectives
Les perspectives de recherche concernent notamment l’évaluation de l’effet cumulatif des séquences thérapeutiques, l’identification de profils de patients à risque oncologique élevé et l’acquisition de données de sécurité à long terme pour les molécules plus récentes, en particulier les inhibiteurs de JAK. L’amélioration des registres et des études en vie réelle devrait permettre d’affiner progressivement la stratification du risque et d’optimiser la prise en charge personnalisée des patients atteints de RIC.
L’auteur déclare avoir des liens d’intérêt avec Pfizer, Bristol Myers Squibb, UCB, Roche, Nordic, Novartis, Sanofi, Boehringer, Abbvie, Chugai, Galapagos/Alfasigma, Biogen, Fresenius Kabi, Sandoz, AstraZeneca, Celltrion.
Bibliographie
1. Avouac J, Fogel O, Beydon M et al. French recommendations for assessing and managing the risk of cancer before the initiation of targeted therapies for chronic rheumatic inflammatory diseases. Joint Bone Spine 2025 : 105944.
2. Beydon M, Pinto S, De Rycke Y et al. Risk of cancer for patients with rheumatoid arthritis versus general population: a national claims database cohort study. Lancet Reg Health Eur 2023 ; 35 : 100768.
3. Karmacharya P, Shahukhal R, Ogdie A. Risk of malignancy in spondyloarthritis: a systematic review. Rheum Dis Clin North Am 2020 ; 46 : 463-511.
4. Crisafulli S, Bertino L, Fontana A et al. Incidence of skin cancer in patients with chronic inflammatory cutaneous diseases on targeted therapies: a systematic review and meta-analysis of observational studies. Front Oncol 2021 ; 11 : 687432.
5. Lee H, Chen SK, Gautam N et al. Risk of malignant melanoma and non-melanoma skin cancer in rheumatoid arthritis patients initiating methotrexate versus hydroxychloroquine: a cohort study. Clin Exp Rheumatol 2023 ; 41 : 110-7.
6. Wolfe F, Michaud K. The effect of methotrexate and anti-tumor necrosis factor therapy on the risk of lymphoma in rheumatoid arthritis in 19,562 patients during 89,710 person-years of observation. Arthritis Rheum 2007 ; 56 : 1433-9.
7. Mercer LK, Lunt M, Low AL et al. Risk of solid cancer in patients exposed to anti-tumour necrosis factor therapy: results from the British Society for Rheumatology Biologics Register for Rheumatoid Arthritis. Ann Rheum Dis 2015 ; 74 : 1087-93.
8. Wadstrom H, Frisell T, Askling J, Anti-Rheumatic Therapy in Sweden Study G. Malignant neoplasms in patients with rheumatoid arthritis treated with tumor necrosis factor inhibitors, tocilizumab, abatacept, or rituximab in clinical practice: a nationwide cohort study from Sweden. JAMA Intern Med 2017 ; 177 : 1605-12.
9. Buchbinder R, Van Doornum S, Staples M et al. Malignancy risk in Australian rheumatoid arthritis patients treated with anti-tumour necrosis factor therapy: analysis of the Australian Rheumatology Association Database (ARAD) prospective cohort study. BMC Musculoskelet Disord 2015 ; 16 : 309.
10. Ytterberg SR, Bhatt DL, Mikuls TR et al. Cardiovascular and cancer risk with tofacitinib in rheumatoid arthritis. N Engl J Med 2022 ; 386 : 316-26.




